Publicaciones SERIDA
Detección de cultivos modificados genéticamente
LUIS J. ROYO. Área de Nutrición, Pastos y Forrajes. ljroyo@serida.org
Introducción
Desde el Neolítico hemos estado modificando los diferentes cultivos para mejorar sus cualidades agrícolas, utilizando la selección y el cruzamiento como herramienta (National Research Council, 2000; Royal Society, 2000). Estas técnicas tradicionales tienen algunas limitaciones, entre las cuales destacan el largo tiempo necesario para lograr los resultados deseados (se necesitan varias generaciones para mejorar un atributo), y su uso limitado dentro de especies relacionadas genéticamente. Sin embargo, otras herramientas, como la tecnología transgénica, aceleran el proceso de mejora permitiendo que un rasgo genético se pueda insertar en una planta seleccionada a través de la introducción directa del gen responsable de ese rasgo. Además, no está restringido por la similitud genética, lo que amplía el número de fuentes potenciales del que se pueden obtener rasgos convenientes (Gelvin, 1998; Royal Society, 1998; Herbers y Sonnewald, 1999; Melchers y Stuiver, 2000).
El potencial de la tecnología transgénica en la agricultura es bien conocido (Ferber, 1999). Actualmente, se están produciendo plantas transgénicas resistentes a patógenos y pesticidas, con calidad nutritiva mejorada, maduración retrasada y mejor sabor (Mazur y col., 1999). Las plantas transgénicas resistentes a parásitos específicos han permitido aumentar las producciones, y debido a la reducción del uso de los pesticidas convencionales suponen un beneficio para el medio ambiente. También son más tolerantes a condiciones de estrés biótico y abiótico, permitiendo su cultivo en tierras marginales.
Detalle mazorca de maíz en estado de floración
¿Qué es un Organismo Modificado Genéticamente?
Podemos definir un organismo modificado genéticamente (OMG, OGM o GMO: Genetically Modified Organism) como cualquier organismo cuyo material genético ha sido modificado de una manera que no se puede producir de forma natural, ni con apareamientos, ni con la recombinación natural. Un caso particular de OMG son los organismos transgénicos, que son organismos a los que se ha introducido en su genoma uno o varios genes procedentes de una especie diferente.
Algunos de los ejemplos de plantas transgénicas que se utilizan más comúnmente son:
Plantas Resistentes a Insectos: Cultivos Bt. El maíz Bt. es un tipo de maíz transgénico que produce una proteína de origen bacteriano, la proteína Cry. Esta proteína es producida de manera natural por la bacteria Bacillus thuringiensis, de donde deriva su nombre “Bt”, y es tóxica para las larvas de insectos barrenadores del tallo, que mueren al comer hojas o tallos de maíz Bt. El taladro del maíz (Diatraea saccharalis y Ostrinia nubilalis) es un lepidóptero que constituye en muchos lugares la principal plaga del cultivo de maíz. Sus larvas se alimentan de los tallos y las hojas, dejando galerías que dañan la planta haciéndola que quebrar, impidiendo el transporte de nutrientes y siendo vía de entrada para hongos.
Las toxinas Bt son consideradas inocuas para mamíferos, pájaros e insectos diferentes al taladro. Los beneficios que presenta el maíz Bt para el agricultor se centran en la posibilidad de controlar las plagas sin recurrir al uso de insecticidas. Sin embargo existen ciertos problemas asociados a su uso, como por ejemplo que otros insectos pueden sustituir a la plaga del taladro en los campos de maíz transgénico (Catangui y Berg, 2006), volviendo al inicio del problema. Un aspecto fundamental a evaluar es cómo afectan las toxinas Bt a los ecosistemas por vías inesperadas, como por ejemplo el hecho de que parte de los residuos agrícolas del maíz Bt puedan contaminar el medio acuático y resultar tóxicos para determinados organismos (Rosi-Marshall, y col., 2007).
Plantas Tolerantes a Herbicidas. La tecnología transgénica se ha usado para introducir transgenes en las plantas que les permitirán tolerar un herbicida específico, normalmente a través de la presencia de una enzima objetivo alterada que es insensible a los pasos clave del herbicida.
El glifosato es un herbicida no selectivo de amplio espectro, desarrollado para la eliminación de hierbas y de arbustos. Inhibe la enzima responsable de la formación de los aminoácidos aromáticos fenilalanina, tirosina y triptófano. Es el principio activo del herbicida Roundup®. Existen ciertos microorganismos que poseen una capacidad de resistencia a la inhibición por glifosato, capacidad que fue utilizada para crear cultivos modificados genéticamente. Concretamente se aisló el gen de la 5-enolpiruvil-shiquimato-3-fosfato sintetasa (EPSPS) de Agrobacterium CP4 resistente a glifosato, se clonó y se transfectó a soja, comenzándose a comercializar desde entonces la soja RR (Roundup® Ready) y posteriormente otros cultivos. La disponibilidad de estos cultivos tolerantes a glifosato (cultivos RR) permite su uso para controlar el desarrollo de especies indeseadas (arvenses) sin afectar el bienestar de la planta. Sin embargo no se puede aplicar a los cultivos que no han sido modificados para tolerarlo, ya que al ser un herbicida de amplio espectro eliminaría tanto a la mala hierba como al cultivo.
Existe gran controversia en el uso del glifosato, así mientras la EPA (Agencia de Protección Ambiental) y la Organización Mundial de la Salud clasificaron los herbicidas con glifosato como de baja toxicidad, algunos trabajos señalan que este compuesto tiene efectos teratogénicos (Benachour y Seralini, 2009; Paganelli y col., 2010).

Los piensos y productos que contengan OMGs deben especificarlo en su etiqueta
El cultivo de maíz modificado genéticamente en España
La autorización y posterior desarrollo de actividades con OMG, incluyendo su cultivo, están claramente regulados tanto en la legislación europea como en la española. A día de hoy a nivel comunitario son sólo dos las variedades de OMG autorizadas para su cultivo, el maíz MON810 (resistente a la plaga de taladro) y la denominada patata “Amflora”, destinada a la producción industrial de almidón. Sin embargo en España, sólo se cultiva el primero de ellos.
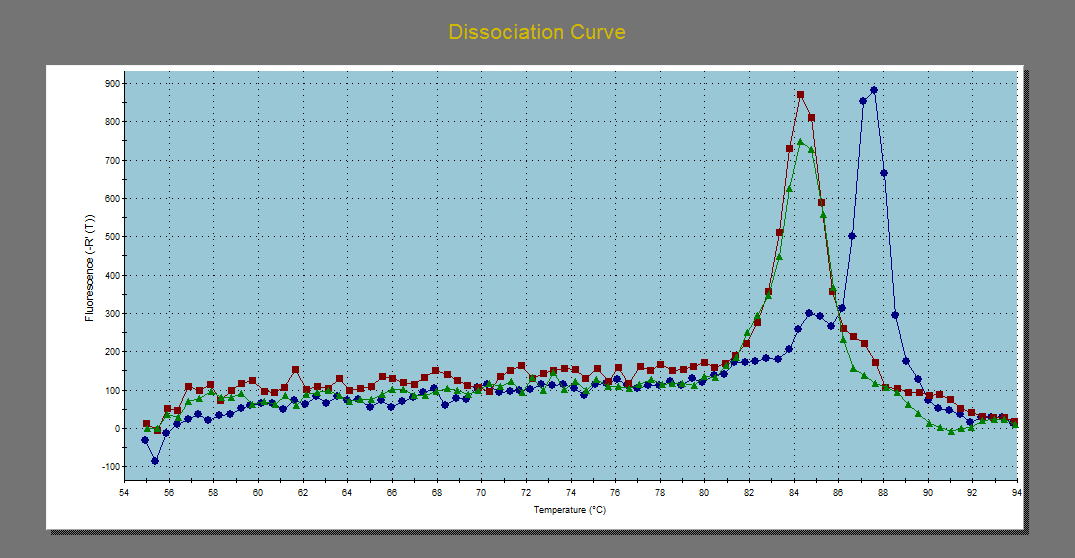
Imagen de las curvas de disociación utilizadas para el diagnóstico de los elementos comunes presentes en construcciones transgénicas.
El cultivo del maíz modificado genéticamente se inició en 1998 con la aprobación de una variedad que contenía el evento 176 de maíz Bt y su inscripción en el Registro Español de Variedades Comerciales. A partir de 2003 comenzaron a comercializarse también otras variedades de maíz Bt que contenían el evento MON 810. En el año 2005, tras la retirada del mercado del evento 176, las variedades del evento MON 810 quedaron cómo las únicas que se cultivan actualmente en España.
En cuanto a su distribución en las diferentes CCAA, la presencia de maíz modificado genéticamente es especialmente relevante en aquellas en las que la plaga del taladro tiene una mayor incidencia. Por este motivo las CCAA con mayor superficie destinada al cultivo de este maíz son Aragón y Cataluña, dónde se encontraría más del 65% de la superficie potencialmente sembrada con semillas de esta variedad de maíz (Figura 1). En estas estadísticas oficiales del MAGRAMA no aparecen datos referentes al Principado de Asturias, ni a sus comunidades limítrofes, considerándose que la superficie cultivada con maíz transgénico es despreciable o nula (http://www.magrama.gob.es/es/calidad-y-evaluacion-ambiental/temas/biotecnologia/organismos-modificados-geneticamente-omg-/consejo-interministerial-de-ogms/superficie.aspx).
.png)
Fig. 1. Contribución de las CCAA a la superficie estimada de siembra de maíz OGM en 2013 (Datos MAGRAMA, 2013).
Detección de OMG
A pesar de su amplio uso, las cosechas genéticamente diseñadas se han encontrado con una gran oposición fundamentalmente en Europa (Christie, 1999; Dale, 1999; Nature, 1999), debido fundamentalmente a los temores sobre la seguridad de los alimentos. Una proporción importante del consumidor europeo no está convencida de que los alimentos derivados de las cosechas de OMGs sean seguros, tanto para el consumidor como para el medioambiente. Estas preocupaciones acerca de los alimentos OMGs contrastan con la aceptación y uso extendidos de muchos productos recombinantes empleados en el cuidado de la salud, como por ejemplo la insulina humana y la hormona de crecimiento, la eritropoyetina, la vacuna de la hepatitis B, el activador de plasminógenos de tejidos, los interferones, el factor VIII o el factor anti hemofílico, entre otros (Dixon, 1999).
El desarrollo y comercialización de cultivos modificados genéticamente ha aumentado dramáticamente en los últimos años debido a los beneficios potenciales descritos anteriormente. Sin embargo, no están exentos de un cierto riesgo medioambiental asociado a su uso, que debe ser correctamente evaluado. Otro problema añadido es la posible presencia de mezclas accidentales de semillas OMG en lotes de semillas libres de OMG, hecho que afecta de manera considerable al mercado global de semillas.
Por estas razones se hace necesario el desarrollo y validación de métodos capaces de detectar la presencia de semillas OMG de una forma fiable, eficaz y económica, y no solo eso, sino también su identificación y cuantificación, fundamentalmente en lotes libres de OMG.
Los test de presencia de OMG se pueden diseñar teniendo en cuenta que son dos las posibles moléculas diana: a) el ADN transgénico que ha sido insertado, mediante técnicas biotecnológicas, en el genoma de una planta natural, o b) la proteína expresada por ese ADN transgénico insertado. Las técnicas basadas en la detección del ADN son las de elección por muchas causas, siendo probablemente la más importante su estabilidad, ya que permite su detección incluso en productos alimentarios procesados.
La técnica de la reacción en cadena de la polimerasa (PCR) es la herramienta más utilizada para la detección y cuantificación de presencia de cultivos modificados genéticamente en alimentos y raciones para el ganado. El factor clave que determina la especificidad de la PCR es la elección del fragmento o secuencia de ADN diana en el genoma de la planta modificada sobre el que va dirigido el protocolo que empleemos. De esta manera se pueden distinguir desde un punto de vista técnico al menos tres categorías, que de menor a mayor especificidad son los siguientes:
Element-specific methods: estos métodos van dirigidos a la detección de secuencias que son comunes en muchas construcciones de transgénesis, y que por lo tanto están presentes en muchos OMG, como es el caso del promotor del virus del mosaico 35S de coliflor, o el terminador nopaline sinthase.
Construct-specific methods: estos métodos van dirigidos a la detección de una secuencia que incluye la unión entre dos elementos adyacentes en una construcción transgénica.
Event-specific methods: en este caso la diana del método abarca una secuencia única situada en la unión entre el genoma de la planta y el ADN recombinante de la construcción transgénica. Es el más específico de los tres métodos.
En la Unión Europea, los productos que contienen OMGs o derivados de éstos, deben ser etiquetados como tales. La única excepción se da cuando su presencia es accidental o inevitable. En este último caso, se permite que el nivel de presencia de OMG llegue hasta el 0,9 % por ingrediente, de tal forma que si el nivel excede el permitido, el producto debe ser etiquetado como producto con OMG. Además la ley obliga a que los productores de estos OMG aporten un método Event-specific (recordamos que es el más específico) para su detección, lo que quiere decir que todos los productos que contienen OMG pueden ser diagnosticados utilizando un protocolo específico y publicado.
Cuando el interés radica en realizar un estudio para la detección de OMG en general (no de un material concreto), los métodos de elección son los basados en la identificación de elementos comunes a muchas construcciones transgénicas para aumentar el espectro de detección. Aunque la completa seguridad de detección de OMG sólo se obtendría utilizando todos los métodos event-specific, combinando la detección simultánea de varios elementos comunes (element-specific) se puede conseguir una probabilidad alta de detección de OMG y a la vez baja de obtener falsos negativos. Además el uso de métodos event-specific es muy caro, con lo que la técnica de elección para hacer un barrido general es la detección simultánea y combinada de varios elementos comunes.
Siguiendo con este razonamiento, en el SERIDA, se está trabajando en el diseño de un protocolo basado en la amplificación de ADN para la detección simultánea de los cinco elementos comunes más utilizados en construcciones transgénicas: Promotor del Cauliflower Mosaic virus 35S (CaMv-P35S), Gen de la Neomycin phosphotransferasa II (nptII), Terminador del gen Nopaline Synthase (T-Nos), promotor del Figwort Mosaic virus 35S (PFMV) y el gen Phosphinothricin N-acetiltransferase (bar).
Este protocolo está en proceso de validación, para la determinación de su límite de detección. Para considerarlo válido, deberá permitir la detección de más del 90% de todos los cultivos comercializados como OMG independientemente del evento de que se trate, y tener un límite de detección menor al 1% para permitir controlar el correcto etiquetado de los productos (piensos o semillas) según establece la Unión Europea.
Referencias bibliográficas
BENACHOUR, SERALINI, Glyphosate Formulations Induce Apoptosis and Necrosis in Human Umbilical, Embryonic, and Placental Cells Chem. Res. Toxicol., 2009, 22 (1): 97–105.
CATANGUI M.A. & BERG R.K. Western bean cutworm, Striacosta albicosta (Smith) (Lepidoptera: Noctuidae), as a potential pest of transgenic Cry1Ab Bacillus thuringiensis corn hybrids in South Dakota. Environmental Entomology 2006, 35: 1439-1452.
CHRISTIE B. Scientists call for moratorium on genetically modified foods. BMJ. 1999; 318:483.
DALE PJ. Public reactions and scientific responses to transgenic crops. Curr Opin Biotechnol. 1999, 10: 203-208.
DIXON B. The paradoxes of genetically modified foods. BMJ. 1999, 318: 547-548.
FERBER D. GM crops in the cross hairs. Science. 1999, 286: 1662-1666.
GELVIN SB. The introduction and expression of transgenes in plants. Curr Opin Biotechnol. 1998, 9: 227-232.
GIANESSI L, CARPENTER J. Agricultural biotechnology: insect control benefits. Washington, DC: National Center for Food and Agricultural Policy; 1999.
HERBERS K, SONNEWALD U. Production of new/modified proteins in transgenic plants. Curr Opin Biotechnol. 1999;10:163-168.
MAZUR B, KREBBERS E, TINGEY S. Gene discovery and product development for grain quality traits. Science. 1999, 285: 372-375.
MELCHERS LS, STUIVER MH. Novel genes for disease resistance breeding. Curr Opin Plant Biol. 2000, 3: 147-152.
Nature Opinion. Time to grasp the international perspective on GM crops. Nature. 1999, 399: 715.
National Research Council. Genetically modified pest-protected plants: science and regulation. Washington, DC: National Academy Press; 2000.
PAGANELLI, GNAZZO V., ACOSTA H., LOPEZ S.L., CARRASCO A.E.. Glyphosate-Based Herbicides Produce Teratogenic Effects on Vertebrates by Impairing Retinoic Acid SignalingChem. Res. Toxicol., 2010, 23 (10): 1586–1595.
ROSI-MARSHALL, E.J., TANK, J.L., ROYER, T.V., WHILES, M.R., EVANS-WHITE, M., CHAMBERS, C., GRIFFITHS, N.A., POKELSEK, J. STEPHEN, M.L. Toxins in transgenic crop byproducts may affect headwater stream ecosystems. Proceedings National Academy of Sciences of the USA 2007, 104(41): 16204-8.
Royal Society, United States National Academy of Sciences, Brazilian Academy of Sciences, et al. Transgenic plants and world agriculture. Washington, DC: National Academy Press; 2000.
| Ficha Bibliográfica | |
|---|---|
| Título | Detección de cultivos modificados genéticamente |
| Autor/es | LUIS J. ROYO. Área de Nutrición, Pastos y Forrajes. ljroyo@serida.org |
| Año Publicación | 2013 |
| Área | |
| Revista/Serie | Tecnología Agoalimentaria. Boletín informativo del SERIDA |
| Referencia | N.12.pp.40-44 |
| Formato | |
| Depósito Legal | As-2.617/1995 |
| ISSN | 1135-6030 |
| ISBN | |
| Ver/Descargar | http://www.serida.org/publicacionesdetalle.php?id=5573&anyo= |

