Publicaciones SERIDA
Control de la paratuberculosis bovina: nuevos métodos de diagnóstico basados en la detección de biomarcadores bovinos
ROSA CASAIS GOYOS. Área de Sanidad Animal. SERIDA
CRISTINA BLANCO VÁZQUEZ. Área de Sanidad Animal. SERIDA
NATALIA IGLESIAS. Área de Sanidad Animal. SERIDA
ANA BALSEIRO MORALES. Universidad de León. Instituto de Ganadería de Montaña.
FERNANDO VICENTE. Área de Nutrición, Pastos y Forrajes. SERIDA
JAVIER AMADO FERNÁNDEZ. Área de Microbiología. Laboratorio de Sanidad Animal Principado de Asturias.
MARÍA CANIVE. DEPARTAMENTO DE SANIDAD ANIMAL. Grupo de Investigación en Micobacterias. NEIKER- Instituto Vasco de Investigación y Desarrollo Agrario.
RAMÓN A. JUSTE. DEPARTAMENTO DE SANIDAD ANIMAL. Grupo de Investigación en Micobacterias. NEIKER- Instituto Vasco de Investigación y Desarrollo Agrario.
MARTA ALONSO-HEARN. DEPARTAMENTO DE SANIDAD ANIMAL. Grupo de Investigación en Micobacterias. NEIKER- Instituto Vasco de Investigación y Desarrollo Agrario.
Antecedentes
La agricultura y la ganadería constituyen dos actividades esenciales en el ámbito económico y social del medio rural en Asturias. En este contexto, cabe destacar la importancia estratégica de la sanidad animal, ya que garantiza la salud y el bienestar animal, la salud pública, la seguridad alimentaria, la producción sostenible de alimentos y la conservación del medio ambiente (Rodríguez García y col., 2014). Además, la Sanidad Animal garantiza la sostenibilidad y competitividad de la producción ganadera y la economía rural, puesto que las enfermedades son responsables del 20% de las pérdidas de la producción animal y constituyen una de las barreras al comercio de animales vivos y alimentos de origen animal.
La PTB es una enteritis granulomatosa crónica muy contagiosa, causada por Mycobacterium avium subsp. paratuberculosis (MAP). Es uno de los principales procesos patológicos que afectan a los rumiantes domésticos y silvestres en la Cornisa Cantábrica (Balseiro et al., 2008. Esta enfermedad es responsable de importantes pérdidas económicas en la industria láctea debido a que produce una disminución significativa de la producción de leche, el adelgazamiento progresivo de los animales, el aumento de los costes veterinarios y el sacrificio prematuro de los casos clínicos. Un estudio realizado en España mediante test ELISA en muestras de leche de tanque estimó que el 18% de las explotaciones lecheras estaban infectadas (Sevilla et al., 2002). En Asturias, en 2019, el 32,6% de las explotaciones de ganado vacuno y el 1,9% de los individuos analizados mediante ELISA para la detección de anticuerpos específicos frente a MAP, estaban infectados (datos aportados por la Consejería de Medio Rural y Cohesión Territorial del Principado de Asturias). Por ello, es una enfermedad que preocupa tanto a ganaderos como a veterinarios.
La PTB bovina se manifiesta bajo un amplio espectro de formas de infección que van desde formas latentes generalmente asintomáticas y caracterizadas por la presencia de lesiones histológicas focales en el tejido intestinal, a formas más severas de la enfermedad, en las que las lesiones granulomatosas son claramente patentes (lesiones multifocales y difusas) (Vázquez et al., 2014), presentando entonces el animal los signos clínicos típicos asociados con la PTB. Estos signos consisten en trastornos diarreicos (intermitentes al principio y progresivamente más severos) y pérdida de peso progresiva (Figura 1). Varios estudios afirman que los terneros son más susceptibles a la infección volviéndose más resistentes con la edad (Larsen et al., 1962). La base de estas diferencias de susceptibilidad dependientes de la edad no ha sido bien documentada, sin embargo, su correcta comprensión es fundamental para el desarrollo de programas de control efectivos (Mortier et al., 2013). La PTB es una enfermedad intestinal crónica de curso predominantemente subclínico. Una vez infectados los animales pueden no manifestar signos clínicos durante un largo periodo de tiempo (2-10 años), pero mientras tanto pueden estar eliminando MAP en las heces, calostro y leche, y, por lo tanto, transmitiendo la enfermedad a otros animales en la ganadería (Bastida y Juste, 2011), originando importantes pérdidas económicas en las explotaciones y haciendo muy difícil el control de la enfermedad.

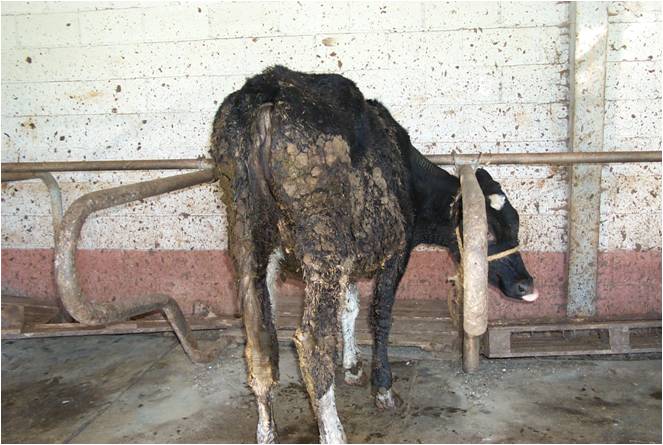
Figura 1. Vacas mostrando distintos signos clínicos típicos (pérdida de peso y diarrea) de la PTB.
El control de la PTB bovina se ha visto obstaculizado por la falta de tratamientos y herramientas de diagnóstico efectivos (Barkema et al., 2017) (ver Figura 2). Asimismo, las vacunas frente a la PTB bovina son vacunas terapéuticas, que evitan la aparición de casos clínicos de la enfermedad, pero que no son capaces de prevenir la infección (Alonso-Hearn et al., 2012). Estas vacunas reducen la severidad de las lesiones histopatológicas, la presencia de MAP en heces y tejidos, y las pérdidas económicas debidas a la disminución de la producción de leche y al acortamiento de la vida productiva del ganado en las explotaciones infectadas. Sin embargo, la prohibición del uso de la vacunación frente a la PTB bovina por parte de las autoridades sanitarias competentes (Directiva 78/52/CEE) debido a su interferencia con los Programas de Erradicación de la Tuberculosis Bovina ha hecho necesaria la búsqueda de nuevas estrategias de control de la PTB. Actualmente, el control de la PTB a nivel de rebaño se basa fundamentalmente en el saneamiento, así como en la prevención de la transmisión de MAP a animales susceptibles usando medidas higiénico-sanitarias adecuadas (Garry, 2011). El saneamiento consiste en la identificación de los animales infectados, especialmente animales asintomáticos que no manifiestan signos clínicos pero que están infectados y eliminan MAP al medio ambiente, y su retirada del grupo para suprimir las fuentes de infección y maximizar la vida productiva del resto de los animales. Por ello, la eficacia de estos programas de control está fuertemente condicionada por los métodos de diagnóstico utilizados para la detección de los animales infectados. Los ensayos diagnósticos ante-mortem actuales (ver Tabla 1 y apartado de definiciones) carecen de la sensibilidad necesaria para ser utilizados como herramientas diagnósticas en infecciones latentes, ya que la carga bacteriana y los niveles de anticuerpos que producen los animales en estas formas de infección son bajos mientras en infecciones patentes son más altos y frecuentemente detectables (Bastida y Juste, 2011). Aunque existen otros factores (Barkema et al., 2017) que han impedido el éxito de los programas de control de la PTB, está claro que la detección de infecciones latentes sigue siendo un desafío y se necesitan nuevas herramientas de diagnóstico para poder controlar la propagación de la enfermedad, así como vacunas eficaces que no interfieran con el diagnóstico de la TB bovina. Otra posible estrategia de control de la enfermedad es la selección de animales con un perfil genético resistente a la infección mediante la inclusión de la PTB en los programas de mejora genética de la raza frisona.
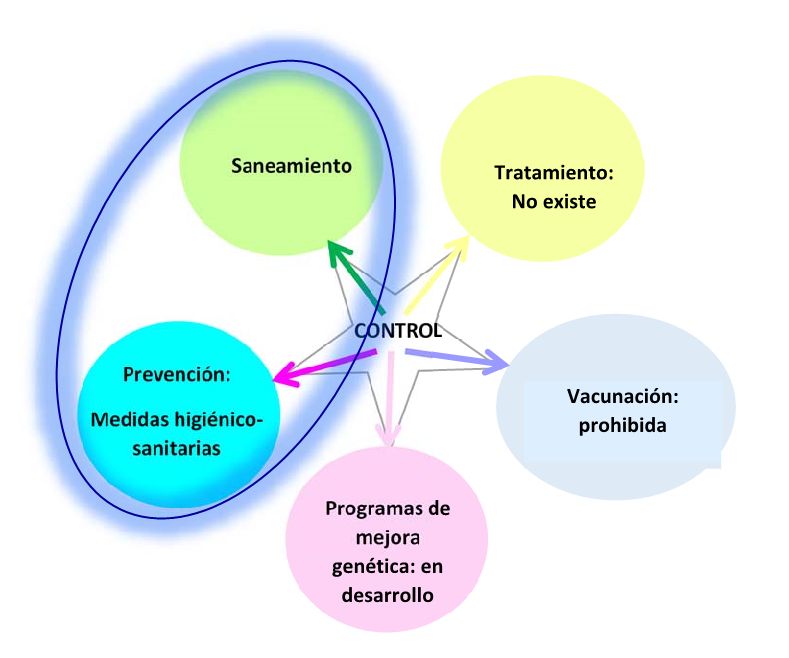
Figura 2. Posibles estrategias para el control de la PTB bovina.
Tabla 1. Métodos utilizados actualmente para el diagnóstico de la PTB
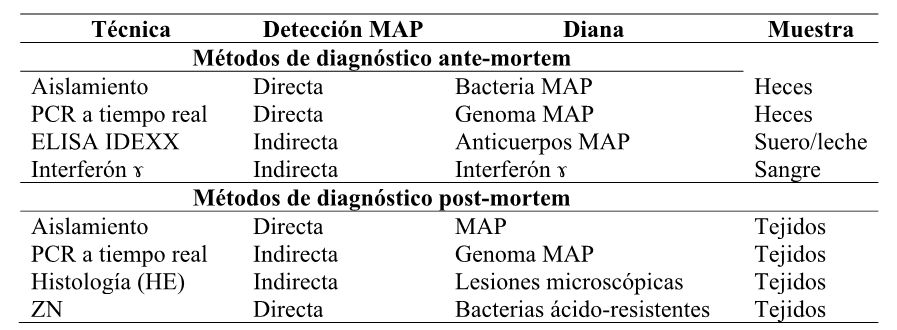
El aislamiento y cultivo de MAP es la técnica de diagnóstico de referencia de la PTB; la PCR a tiempo real más generalizada y eficiente detecta dos dianas: un gen de copia única (F57) y una secuencia de inserción multicopia (IS900); Histología (HE): tinción hematoxilina-eosina del tejido intestinal e identificación de las lesiones granulomatosas típicas; ZN: tinción de Ziehl-Neelsen y visualización de los bacilos ácido-alcohol resistentes de MAP. Ver definiciones de las distintas técnicas de diagnóstico en el apartado correspondiente.
Planteamiento del estudio
Frente a las metodologías clásicas emergen nuevas tecnologías que se están utilizando para el desarrollo de métodos más eficientes de diagnóstico, inmunización y tratamiento de la paratuberculosis. Entre éstas destacan las nuevas tecnologías “ómicas” como la transcriptómica y proteómica, que ofrecen una alternativa para abordar la detección de las distintas formas latentes y patentes en las que se presenta la infección mediante la identificación de biomarcadores asociados a las mismas (ver apartado de definiciones). Estas tecnologías emergentes tienen un enorme potencial porque posibilitan a través de la identificación de biomarcadores el estudio de la patogénesis de la enfermedad a nivel molecular y celular, y pueden ser aplicadas para el desarrollo de herramientas de diagnóstico específicas (biomarcadores de diagnóstico), para monitorizar el curso y predecir el desenlace de la enfermedad (biomarcadores de pronóstico), para predecir la respuesta a tratamientos terapéuticos e intervenciones basadas en vacunas (biomarcador predictivo) y para el desarrollo de terapias (biomarcador terapéutico) (Seth et al., 2009; Carlomagno et al., 2017).
Para abordar el estudio que presentamos aquí partimos de los resultados obtenidos en el proyecto RTA2014-00009-C02-00 en el que utilizamos el análisis transcriptómico para seleccionar 5 biomarcadores bovinos con altos niveles de expresión en sangre de animales infectados con lesiones focales y difusas frente a animales control no infectados sin lesiones (Tabla 2) (Alonso-Hearn et al., 2019).
Tabla 2. Expresión diferencial de los genes codificadores de los biomarcadores seleccionados mediante análisis transcriptómico de sangre periférica de vacas de la raza frisona con lesiones histológicas de tipo focal o difuso frente a vacas control sin lesiones detectadas.
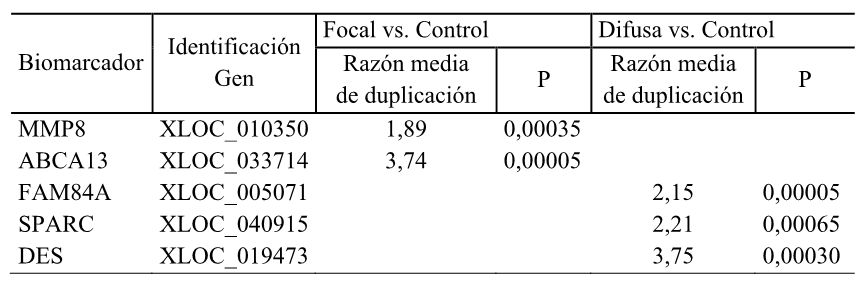
La razón media de duplicación (del inglés “mean Log2 fold change”) es una medida (ratio o razón) de las diferencias en los niveles de expresión de un gen entre dos formas de infección de la PTB, expresado como un logaritmo; MMP8, Matriz Metalopeptidasa 8; ABCA13, proteína de unión a ATP subfamilia A miembro 13; FAM84A, proteína con similitud de secuencia con el miembro 84A; SPARC, proteína secretada acídica y rica en cisteína; DES, Desmina.
El objetivo principal del presente estudio es evaluar el potencial diagnóstico de ELISAs comerciales basados en la detección específica de esos cinco biomarcadores bovinos para detectar formas latentes y patentes de infección de MAP en ganado vacuno infectado de forma natural, utilizando muestras séricas de animales de referencia (n=155) procedentes de nuestras ganaderías colaboradoras. Las muestras se recogieron a partir de 94 animales sacrificados procedentes de ganaderías con alta prevalencia de PTB y 61 animales obtenidos en una ganadería libre de PTB.
Resultados
El estado infeccioso de los animales utilizados en este estudio se valoró en base a su caracterización microbiológica, inmunológica e histopatológica (Tabla 3). Se tomaron muestras de sangre, heces y tejidos de todos los animales sacrificados y muestras de sangre y heces de los animales vivos de la ganadería libre de PTB. El examen patológico de las secciones del tejido intestinal permitió la observación de las lesiones macroscópicas (ver Figura 3) y la clasificación de los animales en cuatro grupos según el tipo y la extensión de las lesiones microscópicas (González et al., 2005; revisado en Balseiro et al, 2019): focal (n=55, 58,51%), multifocal (n=18, 19,14%), difuso (n=15, 15,95%) y sin lesiones histológicas detectables (n=6, 6,38%) (ver Figura 4). Los distintos grupos histopatológicos son un reflejo de las distintas formas de infección en las que se manifiesta la PTB y corresponden con las formas epidemiopatogénicas (Vázquez et al, 2014) que expresan la transmisibilidad y el impacto patológico como aparentemente libres (sin lesiones), latentes (focales) y patentes (multifocales y difuso). En el grupo de animales con lesiones focales, el 76,36% resultaron positivos por uno o varios de los métodos de diagnóstico utilizados (ver Tabla 1) mientras que el resto fueron negativos por todas las técnicas salvo la histología, no mostrando ninguno de los animales de este grupo focal signos clínicos asociados con la enfermedad. En el grupo de animales con lesiones multifocales, el 100% de los animales fueron positivos al menos por una de las técnicas empleadas, por ejemplo, el 94,44% de los animales fueron positivos por ZN. En este grupo el 21,43% de los animales presentaron signos clínicos. Por último, en el grupo con lesiones difusas, el 100% de los animales fueron positivos por ZN, y el 73,33% resultaron positivos por tres métodos (ELISA de anticuerpos, y PCR a tiempo real de heces y tejidos). En este grupo se observó la mayor proporción de animales con signos clínicos asociados a la PTB (64,28%). Sólo 6 animales de los 94 analizados mediante histopatología no mostraron lesiones detectables. Dada la dificultad que tuvimos para encontrar animales sin lesiones se decidió establecer para el estudio un grupo control no-infectado formado por estos 6 animales sin lesiones y los 61 animales de la ganadería libre de PTB.
Tabla 3. Valoración del estado infeccioso (PTB) de las 155 vacas de raza frisona incluidas en el estudio.
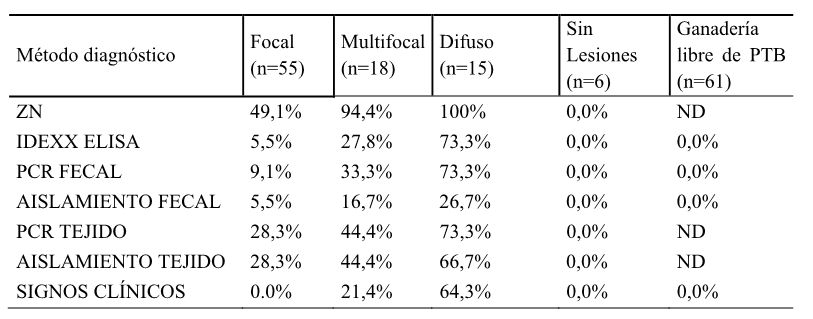
ND, no determinado (animales vivos, no hay disponibilidad de tejidos para realizar esas pruebas diagnósticas); El cálculo del porcentaje de animales que muestran signos clínicos se basa únicamente en aquellos animales en los que se conocía su estado clínico (focal n=28, multifocal n=14, difuso n=14, sin lesiones n=4 y ganadería libre de PTB n=61). Ver definiciones de los distintos métodos de diagnóstico en el apartado correspondiente.
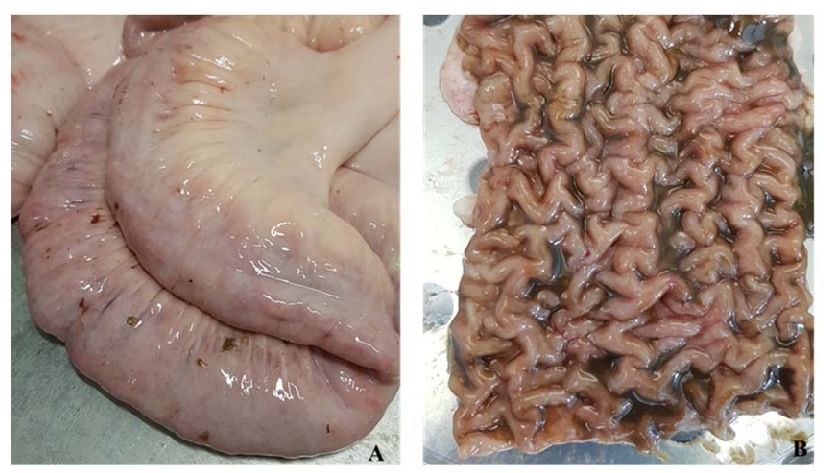
Figura 3. Lesiones macroscópicas en una vaca frisona con lesiones difusas. La pared intestinal aparece muy engrosada, lo que le otorga al intestino un aspecto externo de tubo de goma (A). La mucosa y la submucosa intestinal presentan gruesos pliegues que asemejan las circunvoluciones cerebrales con una ligera congestión en los ápices de los mismos (B).
Una vez valorado el estado infeccioso de los animales se investigó la concentración de cada biomarcador bovino (MMP8, ABCA13, FAM84A, SPARC y DES) en ng/mL en muestras de suero de los 155 animales mediante ELISAs comerciales diseñados específicamente para la detección de dichos biomarcadores (Figura 5). Los datos obtenidos en los 5 ELISAs se evaluaron mediante análisis ROC (del inglés “Receiver Operating Characteristic Curve”) para determinar el punto de corte, la sensibilidad y la especificidad de cada ELISA (ver apartado de definiciones). Además, los resultados obtenidos se compararon con los obtenidos con la prueba comercial de referencia utilizada para la detección específica de anticuerpos anti-MAP, el ELISA de IDEXX. Los resultados de este análisis ROC (Tabla 4) indicaron que el ELISA basado en la detección del biomarcador ABCA13 proporciona el mejor valor diagnóstico para la detección de animales con lesiones focales (sensibilidad 79,25% y especificidad 93,44%); el ELISA basado en la detección del biomarcador SPARC para la detección de animales con lesiones multifocales (sensibilidad 66,70% y especificidad 95,10%); y el ELISA basado en la detección del biomarcador MMP8 para la detección de animales con lesiones difusas (sensibilidad 100,00% y especificidad 77,10%). Para la detección global de animales con cualquier tipo de lesión el ELISA basado en la detección del biomarcador ABCA13 (sensibilidad 70,60% y especificidad 91,80%) superó el valor diagnóstico de todos los biomarcadores e incluso el del ELISA comercial de IDEXX (sensibilidad 28,40% y especificidad 100%).
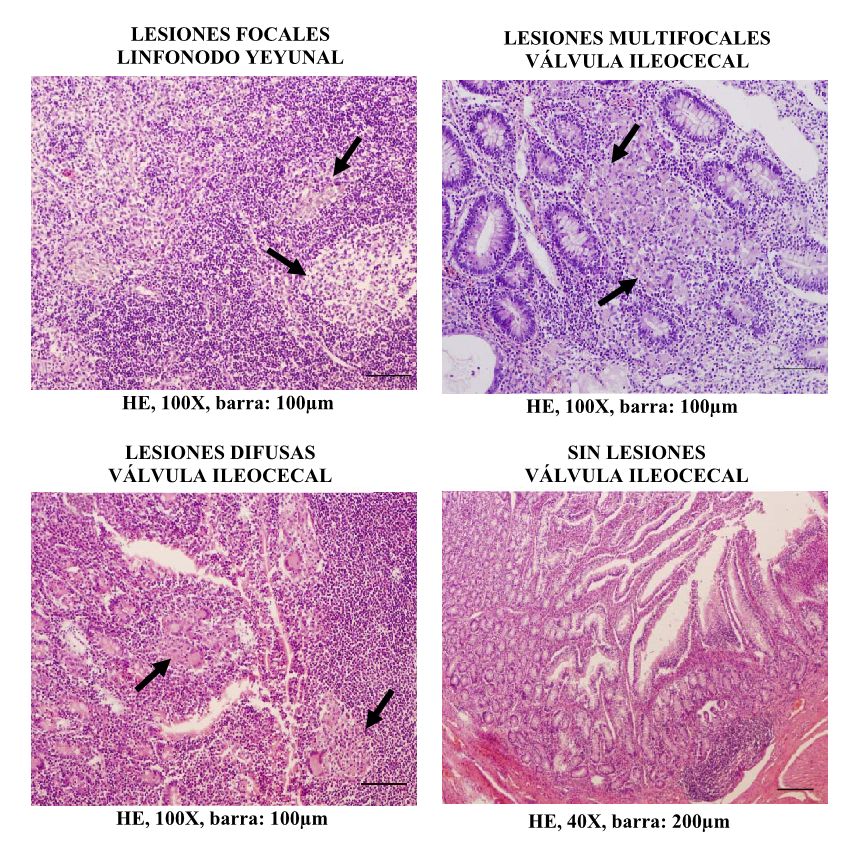
Figura 4. Clasificación histopatológica de los animales. Los animales incluidos en este estudio se clasificaron, de acuerdo con la presencia-ausencia, localización y extensión de las lesiones presentes en los tejidos intestinales en grupo focal, multifocal, difuso y sin lesiones. Las fechas indican la localización de granulomas de PTB.
El valor diagnóstico del biomarcador ABCA13 se mantuvo para todas las categorías histopatológicas de animales infectados, mejorando ampliamente las prestaciones de cualquier prueba de diagnóstico actualmente disponible. Por ello, su uso en los programas de control de la PTB permitiría una detección rápida y sensible de infecciones latentes y patentes, impidiendo la transmisión de MAP a otros animales de la explotación y

Figura 5. ELISA basado en la detección del biomarcador bovino ABCA13.
Tabla 4. Valor diagnóstico de los ELISAs basados en la detección de los biomarcadores seleccionados para el diagnóstico de ganado con diferentes tipos de lesiones histopatológicas en tejido intestinal. Comparación con los resultados obtenidos con el ELISA de IDEXX para la detección específica de anticuerpos anti-MAP.
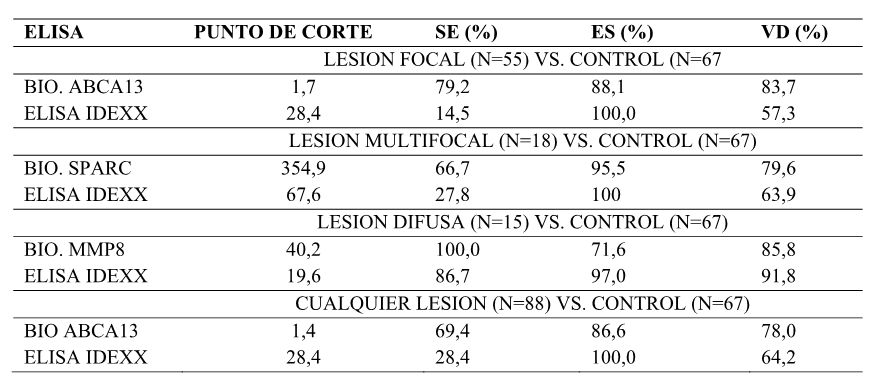
SE, sensibilidad; ES, especificidad; VD, valor diagnóstico (media aritmética de la sensibilidad y la especificidad); N, indica el número de animales por grupo. Ver apartado de definiciones.
Conclusión
Los ELISAs actuales, basados en la detección de anticuerpos específicos frente a MAP, son eficaces en la identificación de animales con infecciones patentes, sin embargo, las infecciones latentes pasan en su mayoría desapercibidas obstaculizando el control de la PTB y su erradicación. La alternativa que hemos presentado en este artículo, los ELISAs basados en la detección de biomarcadores bovinos, y más concretamente el basado en la detección del biomarcador ABCA13, parecen tener el potencial de convertirse en una nueva herramienta de diagnóstico que mejore enormemente la sensibilidad en la detección de animales con formas latentes de infección. No obstante, la limitada casuística a la que se ha aplicado hasta la fecha requiere que se realice una validación a gran escala de este ELISA para confirmar su utilidad en la práctica. Una vez realizada, estos ELISAs podrían utilizarse: 1) en campañas de erradicación para identificar vacas eliminadoras antes de que empiecen a contaminar el medio y transmitir el patógeno, 2) para prevenir la compra de ganado infectado y evitar la difusión de MAP entre ganaderías y 3) para reducir la transmisión potencial de esta micobacteria a otras especies domésticas y animales silvestres susceptibles a la infección.
Definiciones
El aislamiento bacteriológico es un método de detección de bacterias mediante su aislamiento selectivo frente a otros contaminantes y su multiplicación en un medio óptimo que permita el crecimiento necesario para su identificación.
La PCR, reacción en cadena de la polimerasa (del inglés, polymerase chain reaction), es una técnica de amplificación específica de secuencias de DNA diana in vitro. En la actualidad, la versión de PCR más utilizada es la PCR a tiempo real ó PCR cuantitativa. Se utiliza para amplificar y simultáneamente cuantificar el producto de la amplificación específica de un gen o fragmento de ADN diana durante la PCR y no solo al final de la reacción como ocurre en la PCR convencional.
ELISA son las siglas por las que se conoce al ensayo por inmunoabsorción ligado a enzimas (acrónimo del inglés Enzyme-Linked ImmunoSorbent Assay) y es el método estándar actualmente para la realización de pruebas de detección de moléculas orgánicas. Se trata de un método de determinación inmunológica que se basa en el reconocimiento específico entre un antígeno y un anticuerpo, que se detecta y cuantifica por medio de la determinación espectrofotométrica de la acción sobre un sustrato específico de un enzima que va ligado al antígeno o al anticuerpo. Según esté diseñado sirve para detectar/cuantificar la cantidad de anticuerpos específicos frente a un antígeno o la cantidad de antígeno presente en una muestra de suero, sangre, leche, fluido corporal, etc. Esta prueba está limitada en la caso de la paratuberculosis por su baja sensisbilidad, ya que no se desarrollan cantidades suficientes de anticuerpos para ser detectadas hasta las fases más avanzadas de la enfermedad y, aun así, en algunas formas difusas en las que la carga bacteriana es baja, la respuesta de anticuerpos también puede ser débil.
Ensayo del Interferón gamma (IFN-γ), o más precisamente, ensayo de liberación de IFN-γ. Se trata de un método de tipo ELISA sándwich (doble antígeno y/o anticuerpo) que detecta si se ha provocado una respuesta inmune específica mediada por células T cuando la sangre de un individuo se incubada con el antígeno correspondiente. Esta técnica mide la diferencia de señal de IFN-γ para muestras de sangre entera activadas con un extracto antigénico específico de MAP y un antígeno no específico (extracto de M. phlei). Esta técnica refleja que el individuo ha estado expuesto a MAP pero no puede discriminar entre individuos que han controlado la infección e individuos que tienen una enfermedad sub-clínica.
Tinción de Zielh-Neelsen (ZN), es un método de tinción que se utiliza para la detección específica de bacterias ácido alcohol resistentes como las micobacterias en el examen microscópico de muestras de biológicas;
Las tecnologías “Ómicas” derivan su nombre del sufijo “-oma” que, en ciencias biológicas, ha venido a significar aproximadamente “totalidad de un sistema complejo”, y son las disciplinas que analizan el sistema definido por el prefijo. En particular se aplican al análisis global de genes (genómica), mRNA (transcriptómica), proteínas (proteómica) y metabolitos (metabolómica) en diferentes tipos de muestras biológicas bajo determinadas condiciones experimentales.
- La transcriptómica es la rama de la genética que estudia los organismos en términos de su transcriptoma, es decir, el conjunto total de moléculas de ARNm de un organismo bajo determinadas condiciones.
- La proteómica es un área de la biología cuyo objetivo es el estudio de los proteomas. Un proteoma es el conjunto de proteínas expresadas por un genoma, una célula o un tejido. La aplicación de la proteómica tiene un enorme potencial para el desarrollo de métodos de diagnóstico y pronóstico de enfermedades y para la búsqueda de dianas que permitan el diseño de nuevos fármacos y vacunas.
Un biomarcador o marcador biológico es una molécula (ej. ARNm, microARNs y proteínas del hospedador) que puede medirse objetivamente y por la cual se puede identificar un proceso fisiológico o patológico.
Curvas ROC (Burgueño et al., 1995). La calidad de una prueba diagnóstica se juzga por su capacidad para distinguir entre estados alternativos de salud (exactitud). Clásicamente, la exactitud de una prueba diagnóstica se ha evaluado en función de la sensibilidad y la especificidad. Sin embargo, éstas varían en función del criterio elegido como punto de corte entre la población sana y la enferma. Una forma más global de conocer la calidad de la prueba en el espectro completo de puntos de corte es mediante curvas ROC (del inglés-receiver operating characteristics, características operativas del receptor) que constituyen una herramienta fundamental en el proceso de evaluación y uso de pruebas diagnósticas.
El punto de corte de un ELISA, es un valor numérico que define cuando la prueba es positiva o negativa. En función del punto de corte seleccionado para una prueba habrá variación en la sensibilidad y especificidad. Si el punto de corte es alto, la sensibilidad disminuye, porque seremos muy “estrictos” a la hora de identificar un caso positivo. Si se disminuye el punto de corte, la sensibilidad aumenta también, porque nuestro criterio para definir un positivo es muy “laxo”. Sin embargo, la especificidad disminuirá.
La sensibilidad de la técnica nos indica la fracción de verdaderos positivos, es decir, la fracción de animales con lesiones detectadas que es positiva en los ELISAs.
La especificidad de la técnica nos indica la fracción de verdaderos negativos, es decir, la fracción de animales control sin lesiones que es negativa en los ELISAs
Agradecimientos
Este estudio ha sido financiado por el Instituto Nacional de Investigaciones Agrarias (INIA RTA-2014-00009-C02), el Ministerio de Ciencia, Innovación y Universidades (MICINN RTI2018-094192-R-C22), Fondos Europeos para el Desarrollo Regional (FEDER) y fondos regionales PCTI 2018–2020 (GRUPIN: IDI2018-000237). Agradecemos al INIA la financiación de los contratos pre-doctorales de formación de Cristina Blanco Vázquez y María Canive.
Nos gustaría agradecer la asistencia técnica de la Unidad de Asesoramiento Estadístico de los Servicios Científico-Técnicos de la Universidad de Oviedo, la asistencia en los muestreos de nuestras ganaderías colaboradoras y los Servicios Veterinarios ASTEGA y la colaboración de los operarios de campo del SERIDA en la toma de muestras, y el cuidado y mantenimiento de los animales.
Referencias bibliográficas
ALONSO-HEARN, M., MOLINA, E., GEIJO, M., VÁZQUEZ, P., SEVILLA, I.A., GARRIDO, J.M. & JUSTE, R.A. (2012). Immunization of adult dairy cattle with a new heat-killed vaccine is associated with longer productive life prior to cows being sent to slaughter with suspected paratuberculosis. Journal of Dairy Science 95, 618–629.
ALONSO-HEARN, M., CANIVE, M., BLANCO-VÁZQUEZ, C., TORREMOCHA, R., BALSEIRO, A., AMADO, J., VARELA-MARTÍNEZ, E., RAMOS, R., JUGO, B.M. & CASAIS, R. (2019). RNA-Seq analysis of ileocecal valve and peripheral blood from Holstein cattle infected with Mycobacterium avium subsp, paratuberculosis revealed dysregulation of the CXCL8/IL8 signaling pathway. Scientific Reports 9, 14845.
BALSEIRO, A., GARCÍA MARÍN, J.F., SOLANO, P., GARRIDO, J.M. & PRIETO, J.M. (2008). Histopathological classification of lesions observed in natural cases of paratuberculosis in free-ranging fallow deer (Dama dama). Journal of Comparative Pathology 138, 180-188.
BALSEIRO, A., PEREZ, V., JUSTE R.A. Chronic regional intestinal inflammatory disease: A transspecific slow Infection? Comparative Immunology, Microbiology and Infectious Diseases 62, 88-100.
BARKEMA, H.W., ORSEL, K., NIELSEN, S.S., KOWTS, A.P., RUTTEN, V.P.M.G., BANNANTINE, J.P., KEEFE, G.P., KELTON, D.F., WELL, S.J., WHITTINGTON, R.J., MACKINTOSH, C.G., MANNING, E.J., WEBER, M.F., HEURER, C., FORDE, T.L., RITTER, C., ROCHE, S., CORBETT, C.S., WOLD, R., GRIEBEL, P.J. & DE BUCK, J. (2017) Knowledge gaps that hamper prevention and control of Mycobacterium avium subspecies partuberculosis infection. Transboundary and Emerging Diseases 65, 125-148.
BASTIDA, F. & JUSTE, R.A. (2011). Paratuberculosis control: a review with a focus on vaccinarion. Journal of Immune Based Therapies and Vaccines 9, 8.
BURGUEÑO, M.J., GARCÍA-BASTOS, J.L., GONZÁLEZ -BUITRAGO, J.M. (1995). Las curvas ROC en la evaluación de las pruebas diagnósticas. Medicina Clínica 104, 661-670.
CARLOMAGNO, N., INCOLLING, P., TAMMRO, V., PELUSO, G., RUPEALTA, N., CHIACCHIO, G., SANDOVAL SOTELO, M.L., MINIERI, G., PISANI, A., RICCIO, E., SABBATINI, M., BRACALE, U.M., CALOGERO, A., DODARO, C.A. & SANTANGELO, M. (2017). Diagnostic, Predictive, Prognostic, and Therapeutic Molecular Biomarkers in Third Millennium: A Break through in Gastric Cancer. Biomed Research International 2017, 7869802.
GARRY, F. (2011). Control of paratuberculosis in dairy herds. Veterinary Clinics of North America: Food Animal Practice 27, 599–607.
GONZÁLEZ, J., GEIJO, M.V., GARCÍA-PARIENTE, C., VERNA, A., CORPA, J.M., REYES, L.E., FERRERAS, M.C., JUSTE, R.A., GARCÍA MARÍN, J.F. & PÉREZ, V. (2005). Histopathological classification of lesions associated with natural paratuberculosis infection in cattle. Journal of Comparative Pathology 133, 184–196.
LARSEN, A.B., MERKAL, R.S. & SULIP, R.C. (1975). Age of cattle as related to resistance to infection with Mycobacterium paratuberculosis. American Journal of Veterinary Research 36, 255-257.
MORTIER, R.A.R., BARKEMA, H.W., BYSTROM, J.M., ILLANES, O., ORSEL, K., WOLF, R., ATKINS, G. & DE BUCK, J. (2013). Evaluation of age-dependent susceptibility in calves infected with two doses of Mycobacterium avium subspecies paratuberculosis using pathology and tissue culture. Veterinary Research 44, 94.
RODRÍGUEZ GARCÍA, M.J., RANZ CASARES, A., BARREIRO MORÁN, B., DEBECQUE PEÑA, J., SANZ FERNÁNDEZ, A., RUEDA PÉREZ, P. (2014). La biotecnología en Sanidad Animal. Arbor 190(768), A154.
SETH, M., LAMONT, E.A., JANAGAMA, H.K., WIDDEL, A., VULCHANOVA, L., STABEL, J.R., WATERS, W.R., PALMER, M.V. SREEVATSAN, S. (2009). Biomarker discovery in subclinical mycobacterial infections of cattle. PLoS One 4, e5478.
SEVILLA, I., ADURIZ, G., GARRIDO. J.M., GEIJO, M.V., JUSTE RA. A preliminary survey on the prevalence of paratuberculosis in dairy cattle in Spain by bulk milk PCR. 7th International Colloquium on Paratuberculosis. Bilbao, 11-15th june,
VAZQUEZ, P., GARRIDO, J.M., MOLINA, E., GEIJO, M.V., GOMEZ, N., PEREZ, V., SEVILLA, I.A., ALONSO-HEARN, M., CORTES, A., JUSTE, R.A. (2014) Latent infections are the most frequent form of paratuberculosis in slaughtered Friesian cattle. Spanish Journal of Agricultural Research, 12(4): 1049-1060.
WINDSOR, P.A. & WHITTINGTON, R.J. (2010). Evidence for age susceptibility of cattle to Johne’s disease. The Veterinary Journal 184, 37-44.
| Ficha Bibliográfica | |
|---|---|
| Título | Control de la paratuberculosis bovina: nuevos métodos de diagnóstico basados en la detección de biomarcadores bovinos |
| Autor/es | ROSA CASAIS GOYOS. Área de Sanidad Animal. SERIDA CRISTINA BLANCO VÁZQUEZ. Área de Sanidad Animal. SERIDA NATALIA IGLESIAS. Área de Sanidad Animal. SERIDA ANA BALSEIRO MORALES. Universidad de León. Instituto de Ganadería de Montaña. FERNANDO VICENTE. Área de Nutrición, Pastos y Forrajes. SERIDA JAVIER AMADO FERNÁNDEZ. Área de Microbiología. Laboratorio de Sanidad Animal Principado de Asturias. MARÍA CANIVE. DEPARTAMENTO DE SANIDAD ANIMAL. Grupo de Investigación en Micobacterias. NEIKER- Instituto Vasco de Investigación y Desarrollo Agrario. RAMÓN A. JUSTE. DEPARTAMENTO DE SANIDAD ANIMAL. Grupo de Investigación en Micobacterias. NEIKER- Instituto Vasco de Investigación y Desarrollo Agrario. MARTA ALONSO-HEARN. DEPARTAMENTO DE SANIDAD ANIMAL. Grupo de Investigación en Micobacterias. NEIKER- Instituto Vasco de Investigación y Desarrollo Agrario. |
| Año Publicación | 2021 |
| Área | |
| Revista/Serie | Tecnología Agroalimentaria. Boletín informativo del SERIDA |
| Referencia | Nª 24: 22-31 |
| Formato | |
| Depósito Legal | AS2617/1995 |
| ISSN | 1135-6030 |
| ISBN | |
| Ver/Descargar | |

